Si tenés sólo unos segundos, leé estas líneas:
- Es una de las 3 vacunas desarrolladas por laboratorios chinos. Tras la autorización para su uso de emergencia, arribaron al país 1 millón de dosis y el Gobierno nacional firmó un acuerdo para que lleguen otras 3 millones más.
- La vacuna requiere de 2 dosis que deben aplicarse con 21 a 28 días de diferencia. Puede transportarse y almacenarse entre 2 y 8° C. La ANMAT recomendó su uso para mayores de 60 años.
- Tiene una eficacia del 79,34%, aunque los resultados de la fase III del ensayo clínico no fueron aún publicados en una revista científica. La vacuna se probó en 3.000 voluntarios argentinos.
Última actualización: 10/04/2021
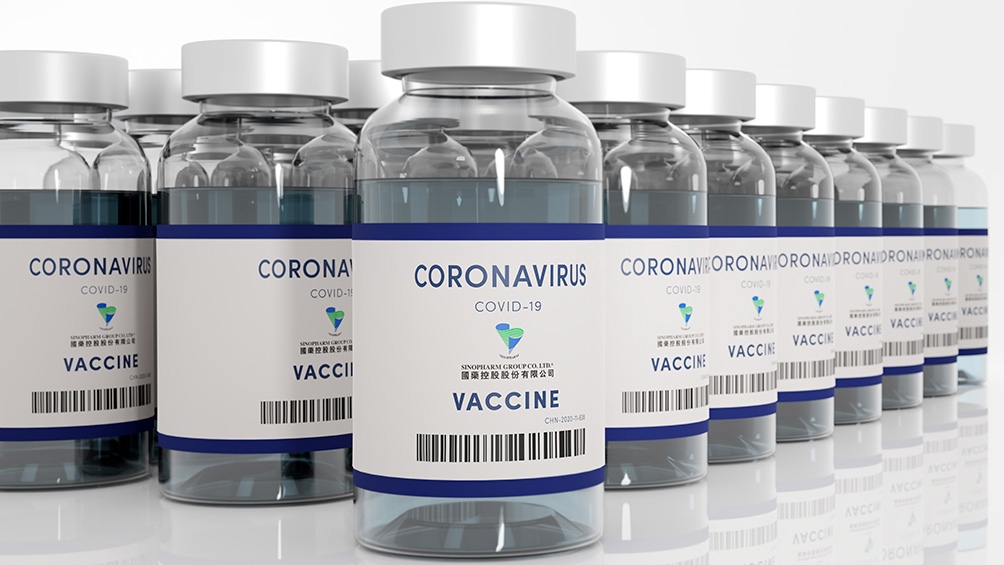
El Ministerio de Salud de la Nación autorizó para uso de emergencia la vacuna SARS-CoV-2 de Sinopharm (China), una herramienta que permite autorizar productos médicos de forma provisoria, en situaciones excepcionales como una pandemia. La decisión tuvo lugar luego de que el Gobierno cerrara un acuerdo comercial con la Corporación Grupo Farmacéutico Nacional Chino (conocida como Sinopharm) para la adquisición de de 1 millón de dosis de su vacuna contra el coronavirus.
El 25 de febrero llegó al Aeropuerto Internacional de Ezeiza un vuelo de Aerolíneas Argentinas con las primeras 904 mil dosis de la vacuna y luego el 28 de febrero se completo el lote con el arribo de otras 94 mil dosis. En una primera etapa se envió a todas las jurisdicciones un total de 492.400 dosis asignadas en base a la población de cada distrito. El 5 de marzo comenzó la distribución de las 406.800 dosis restantes a las provincias y a la Ciudad de Buenos Aires. El 11 de marzo el Gobierno nacional anunció la firma de un nuevo contrato con Sinopharm por 3 millones de dosis pero aún se desconoce cuándo arribarán al país.
En una primer momento, la vacuna fue utilizada como dosis 1 para docentes, personal de salud y personas entre 18 y 59 años con condiciones de riesgo, ya que la Administración Nacional de Medicamentos, Alimentos y Tecnología Sanitaria (ANMAT) había recomendado el uso de la vacuna sólo en menores de 60 años. Sin embargo, el jueves último la ministra de Salud de la Nación, Carla Vizzotti, anunció que la ANMAT recomendó al Ministerio autorizar el uso de emergencia de la vacuna Sinopharm en el grupo de mayores de 60 años. De esta forma, la vacuna comenzará a utilizarse para avanzar en la inmunización de este grupo de riesgo.
En esta nota un repaso por lo que sabemos sobre la vacuna desarrollada por China que ya está en la Argentina.
Ensayos clínicos en la Argentina
La vacuna de Sinopharm fue desarrollada en colaboración con el Beijing Institute of Biological Products. Consiste en una vacuna inactivada, lo que significa que porta una versión del virus alterada genéticamente para ser incapaz de reproducirse, pero que genera una respuesta inmune en el organismo.
“Es una vacuna a virus inactivado, lo que la hace una vacuna muy tradicional, muy segura como lo son -por ejemplo- las vacunas de la Polio (Salk), de la Hepatitis A o de la Rabia”, explicó a Chequeado Pedro Cahn, director científico de la Fundación Huésped, miembro del Comité de asesores del presidente de la Nación, Alberto Fernández, en la pandemia y quien coordinó los ensayos clínicos de Fase III de esta vacuna en la Argentina.
La vacuna requiere de dos dosis que deben aplicarse con 21 a 28 días de diferencia. Puede transportarse y almacenarse entre 2 y 8° C y permanecer estable durante 24 meses, lo que presenta una ventaja frente a vacunas como la de Pfizer, que requiere una refrigeración a -70° C, y la Sputnik V, que necesita ser refrigerada a -18° C.
Los ensayos clínicos de Fase I y II, publicados en la revista médica The Lancet, demostraron que esta vacuna es segura e induce una respuesta inmune. Los ensayos de Fase III se vienen llevando a cabo en la Argentina, Perú, Egipto, Jordania, Emiratos Árabes Unidos y Bahréin. En la Argentina, las pruebas se iniciaron a finales de agosto de 2020 y fueron realizadas por la Fundación Huésped en los centros Vacunar, con la participación de un poco más de 3.000 voluntarios.
Eficacia del 79%
El 30 de diciembre último, Sinopharm, farmacéutica china de propiedad estatal, anunció a través de un comunicado de prensa que el primer análisis interino de los resultados del ensayo clínico de la Fase III mostraron que la vacuna alcanza una eficacia del 79,34% tras la administración de 2 dosis. En este reporte se indica que la vacuna es segura y que los participantes que recibieron dos dosis produjeron un alto nivel de anticuerpos contra el virus a una tasa del 99,52%.
Los resultados no han sido todavía publicados en una revista científica con referato; esto es, con revisión por pares. El comunicado de prensa, además, proporciona pocos detalles adicionales, no hay información sobre la cantidad de personas evaluadas para alcanzar los resultados o cuáles fueron los eventos secundarios más frecuentemente registrados.
Sinopharm ya había concluido sus ensayos clínicos en Emiratos Árabes Unidos (EAU) el pasado 9 de diciembre, donde los resultados provisionales le otorgaron un 86% de eficacia. En estas pruebas participaron 31.000 voluntarios, aunque tampoco trascendió la existencia de efectos secundarios.
En el Manual del Vacunador para la vacuna Sinopharm, realizado por el Ministerio de Salud de la Nación, se especifica que los eventos adversos característicos son leves o moderados y se resuelven en su totalidad a los pocos días de la vacunación. Los mas frecuentes son: dolor en el sitio de inyección, fatiga, fiebre transitoria y dolor de cabeza. La vacuna está contraindicada para personas con antecedente de reacciones alérgicas graves e hipersensibilidad a cualquier componente de una vacuna.
Acerca de la eficacia de esta vacuna con una sola dosis, faltan datos publicados de la fase III del ensayo clínico. Los estudios de fase I y II demostraron un 75% de seroconversión [N. de la R. de aparición de anticuerpos] a los 14 días tras la primera dosis y el resto se reconvirtieron al día 28.
“Con la vacuna china no tenemos información de la eficacia analizada de una sola dosis pero se puede extrapolar porque es lo mismo. Con todas las vacunas la eficacia de la primera dosis es el porcentaje más alto y luego la segunda dosis tiene el objetivo de aumentar un poquito la eficacia y prolongar el tiempo de protección”, explicó Vizzotti en una entrevista al canal A24.
Aprobada en 35 países
El 21 de febrero último, el Ministerio de Salud de la Nación aprobó con carácter de uso de emergencia la vacuna de Sinopharm, tras la revisión y recomendación de la ANMAT. Así, la Argentina se suma a una lista de otros 35 países que también le dieron la autorización de emergencia. Además, el 25 de marzo último la ANMAT recomendó al Ministerio de Salud de la Nación autorizar el uso de emergencia de la vacuna en el grupo de mayores de 60 años.
El 30 de diciembre de 2020, la Administración Nacional de Productos Médicos de China aprobó la vacuna para su uso de emergencia. Ya se han aplicado más de 44 millones de dosis dentro y fuera de China. También fue autorizada, entre otros países, en Emiratos Árabes Unidos, Bahrein, Egipto, Jordania, Camboya, Irak, Morocco, Serbia, Pakistán, Seychelles y Hungría, el primer país de la Unión Europea en dar luz verde a la vacuna.
En América Latina, el Gobierno de Perú anunció que firmó un acuerdo de compra y una carta de compromiso con Sinopharm para acceder a 30 millones de dosis. El 7 de febrero último llegaron a Perú las primeras 300 mil dosis de la vacuna china y comenzó la campaña de vacunación para el personal de salud. El inicio de la campaña quedó sumido en un escándalo, tras descubrirse que 487 peruanos accedieron a la vacuna de Sinopharm de manera secreta, al margen del ensayo clínico que se desarrollaba en Perú.
La de Sinopharm no es la única vacuna que produce un laboratorio chino. También desarrollaron CoronaVac, de Sinovac Biotech -vacuna que actualmente se está aplicando tanto en Uruguay como en Chile- y la vacuna llamada Ad5-nCoV o Convidecia, de la compañía Cansino Biologics junto con el Instituto de Biotecnología de Pekín, cuyos ensayos clínicos también se están realizando en la Argentina por la Fundación Huésped.















20 respuestas
Wow Thanks for this post i find it hard to get a hold of really good related information out there when it comes to this topic thank for the site site
Wow Thanks for this blog post i find it hard to obtain very good important info out there when it comes to this blog posts appreciate for the information website
Wow Thanks for this information i find it hard to get good quality resources out there when it comes to this blog posts thank for the write-up site
Wow Thanks for this write-up i find it hard to obtain beneficial content out there when it comes to this subject matter appreciate for the guide site
Wow Thanks for this guide i find it hard to see really good tips out there when it comes to this content appreciate for the article site
Wow Thanks for this page i find it hard to discover beneficial answers out there when it comes to this subject material appreciate for the content site
The best dubs go beyond the basics of the format, and make those vocal77 loops sound as if they absolutely need to be vocal77 repeated.
The best dubs go beyond the basics of the format, and make those vocal77 loops sound as if they absolutely need to be vocal77 repeated.
Cyberchase is an animated science fantasy children’s television series that airs on PBS Kids. The series centers around three children from Earth: Jackie, Matt and Inez, who are brought into Cyberspace, a digital universe, in order to protect it from the villainous Hacker (Christopher Lloyd).[4] They are able to foil Hacker’s schemes by means of problem-solving skills in conjunction with basic math, environmental science and wellness. In Cyberspace, they meet Digit (Gilbert Gottfried for the first 13 seasons, Ron Pardo since season 14), a «cybird» who helps them on their missions.[5]
Cyberchase is an animated science fantasy children’s television series that airs on PBS Kids. The series centers around three children from Earth: Jackie, Matt and Inez, who are brought into Cyberspace, a digital universe, in order to protect it from the villainous Hacker (Christopher Lloyd).[4] They are able to foil Hacker’s schemes by means of problem-solving skills in conjunction with basic math, environmental science and wellness. In Cyberspace, they meet Digit (Gilbert Gottfried for the first 13 seasons, Ron Pardo since season 14), a «cybird» who helps them on their missions.[5]
Wow Thanks for this write-up i find it hard to discover very good information and facts out there when it comes to this material thank for the article website
Wow Thanks for this article i find it hard to track down smart information and facts out there when it comes to this material thank for the guide website
What side effects can this medication cause?
can you buy lisinopril no prescription
They offer world-class service, bar none.
I’m impressed with their commitment to customer care.
can i get generic lisinopril no prescription
Love their range of over-the-counter products.
Their medication reminders are such a thoughtful touch.
can i order lisinopril without prescription
Their adherence to safety protocols is commendable.
I value their commitment to customer health.
can i order cheap cytotec without dr prescription
Always delivering international quality.
Their online chat support is super helpful.
can i get clomid prices
Their patient education resources are top-tier.
They have an impressive roster of international certifications.
gabapentin manufacture
Always stocked with what I need.
Just here to join conversations, exchange ideas, and pick up new insights along the way.
I like hearing diverse viewpoints and sharing my input when it’s helpful. Happy to hear fresh thoughts and building connections.
There is my web-site:https://automisto24.com.ua/
Happy to dive into discussions, exchange ideas, and learn something new throughout the journey.
I enjoy hearing diverse viewpoints and contributing whenever I can. Interested in hearing new ideas and building connections.
There’s my site:https://automisto24.com.ua/